CAR-T细胞疗法拓宽了某些癌症特别是某些血癌的治疗选择。但它们也有局限性:1)癌细胞上可变的抗原表达模式可能导致“治疗逃逸”;2)CAR-T细胞可能耗竭,甚至被癌细胞本身抑制;3)免疫抑制肿瘤微环境导致CAR-T对致密实体瘤缺乏疗效。迄今为止,CAR-T疗法仅被批准用于B细胞恶性肿瘤的治疗。
现在,来自纪念斯隆-凯特琳癌症中心斯隆-凯特琳研究所(SKI)的科学家们已经开发出一种新型的CAR-T细胞——合成酶武装的杀伤(SEAKER)细胞,其结合了免疫细胞搜寻靶标的能力以及局部生成强效抗癌药物的能力,作用好比“微型制药厂”。
简单来说,这些CAR-T细胞被设计共表达能在疾病部位激活全身递送前药的细菌酶,从而杀死含有癌症标记物的肿瘤细胞和附近不含有癌症标记物的肿瘤细胞。更重要的是,这些工程细胞即使耗竭,酶活性仍持续存在,维持药物生产,而且这些药物不会受到癌症的抑制。这项工作于2021年12月30日发表在Nature Chemical Biology上。
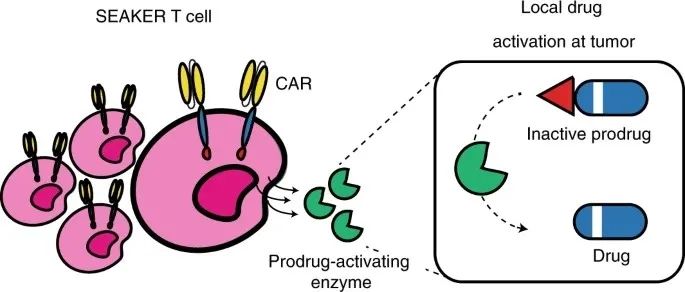
来源:Nature Chemical Biology
利用CAR-T细胞递送额外治疗药物的想法并不新鲜。一些研究小组已经证明,让细胞产生抗体和细胞因子等免疫蛋白是可能的。但让CAR-T细胞生产小分子抗癌药物更具挑战性。
这项研究中使用的5′-O-Sulfamoyladenosine(AMS)是一种具有高度细胞毒性的天然产物,无法直接注射到血液中。但是,当它在肿瘤部位局部产生时,可以有效且安全地杀死小鼠体内的癌细胞。
在这项新研究中,科学家们将AMS与能“掩蔽”其功能的基团连接起来。然后,他们对T细胞进行基因工程,以制造能从药物中切割“掩蔽基团”酶。前药被注射到血液中并在体内循环,而定位于肿瘤部位的CAR-T细胞产生的酶能确保在肿瘤局部释放前药的活性部分。
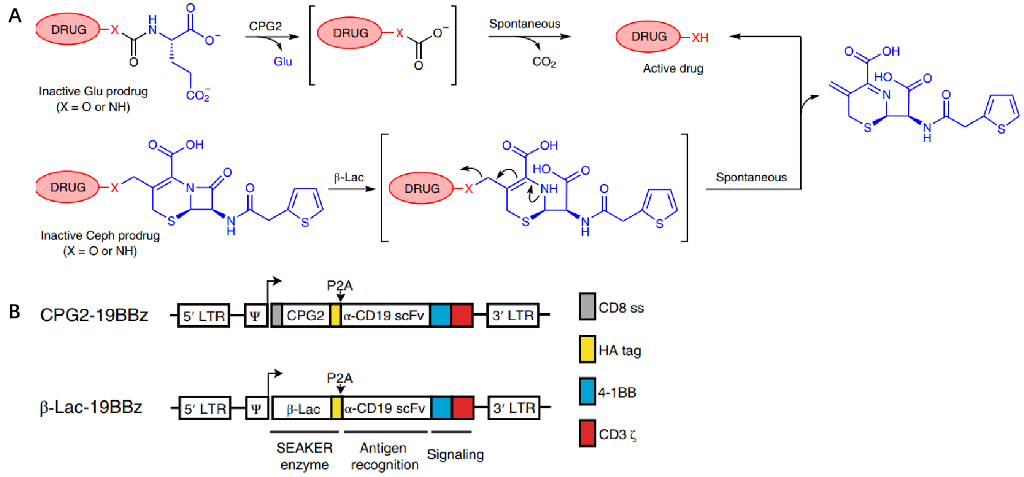
A:用于SEAKER细胞的模块化前药设计。a)谷氨酸(Glu)掩蔽的前药可用假单胞菌CPG2裂解,形成碳酸(X=O)或氨基甲酸(X=NH)酸中间体,然后linker自发分解形成活性药物。b)头孢噻吩(Ceph)掩蔽的前药可被阴沟肠杆菌β-Lac 裂解形成水解中间体,随后自发消除头孢噻吩副产物以形成活性药物。药物以红色显示,掩蔽基团以蓝色显示,linker以灰色显示。
B: SEAKER CAR构建体编码分泌型前药激活酶:CPG2-19BBz (CPG2/α-CD19/4-1BB/CD3ζ) 和β-Lac-19BBz (β-Lac/α-CD19/4-1BB/CD3ζ)。(来源:Nature Chemical Biology)
研究小组分别在体外癌细胞和小鼠模型实验上测试了SEAKER细胞。在这两种情况下,SEAKER细胞+前药在杀死癌细胞方面的表现都优于常规的CAR-T细胞+前药。
此外, 在用SEAKER细胞和前药处理的小鼠中观察到抗原阴性细胞的显著杀伤(下图g,h)。并且即使T细胞耗竭,SEAKER酶活性仍能维持(下图i)。
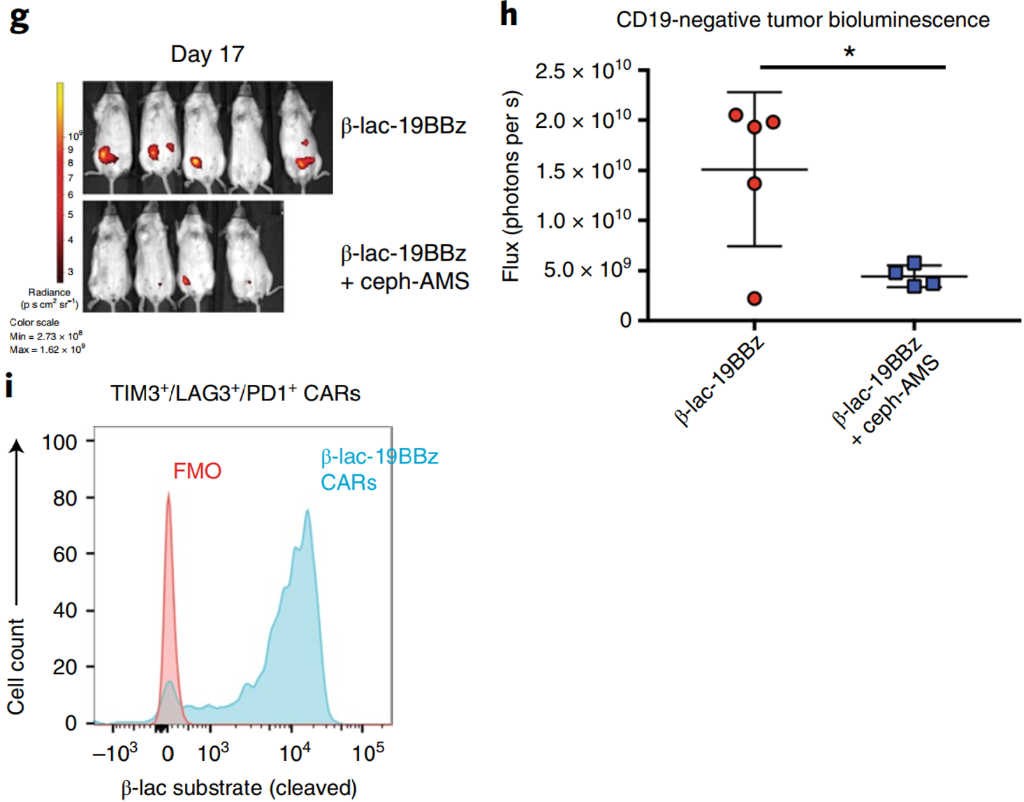
来源:Nature Chemical Biology
CoImmune公司已获得该技术的许可,以开发用于人体试验的新型CAR-T细胞技术。
SEAKER技术的另一个吸引力在于它有不止一种可能的应用:它能被用来生产药物以对抗其他疾病,比如自身免疫性疾病和感染。但目前,SKI研究人员和CoImmune的重点将放在癌症上。Scheinberg推测,癌症的临床试验启动大约需要两到三年的时间。
参考资料:
1# CAR-T SEAKER Cells Activate Small Molecule Drugs at Tumor Site(来源:GEN)
2# Thomas J. Gardner et al. Engineering CAR-T cells to activate small-molecule drugs in situ. Nature Chemical Biology. 2022